|
Estudio histológico de lesiones ateromatosas en aorta de
ratas hembras de 4 meses de edad, con ovario
poliquístico inducido por testosterona
Arizaga, Hugo César
Cátedra de Anatomía y
Fisiología Patológicas. Cátedra de Biología. Facultad de
Ciencias Médicas. Universidad Nacional de Rosario
|
|
INTRODUCCIÓN
Como se
mencionó anteriormente, el papel de la hiperandrogenemia, no
está claro en lo que respecta a sus efectos sobre el riesgo
cardiovascular y las lesiones arteriales. Es esto lo que me
impulsó a llevar a cabo un proyecto de investigación con el fin
de intentar esclarecer el papel de la hiperandrogenemia en las
lesiones arteriales en ratas de 4 meses de edad de la línea “e”.
El
desarrollo de ovarios poliquísticos estaría justificado por la
existencia de diversos estudios en los que se logró la inducción
de ovarios poliquísticos mediante la aplicación de distintas
drogas como: valearato de estradiol, propionato de testosterona,
mefiprestone, a distintas edades, en diferentes dosis y en otras
líneas de ratas.
En lo que
respecta a las alteraciones arteriales que esperaría encontrar,
me he basado en diversos estudios que se han realizado en
distintos animales y que aún no permiten clarificar el papel de
la testosterona en el daño arterial, tanto funcional como
estructural.
Creo
particularmente, que la lesión arterial mediada por andrógenos
estaría justificada, en parte, por la presencia de receptores
para andrógenos tanto en las células musculares lisas de las
arterias de ratas, como en las células inflamatorias, como
algunos estudios lo han demostrado.
En cuanto al papel
desempeñado por los eosinófilos en las enfermedades
cardiovasculares; se han hallado, en necropsias por muerte
súbita por disección coronaria espontánea, en la adventicia de
las arterias afectadas presencia de infiltrados eosinofílicos en
las mismas. Se postula que las proteínas de los gránulos de
éstas células podrían haber dañado el colágeno, la elastina o
las células musculares lisas de las arterias afectadas por la
disección.
Se sabe que la
disección coronaria, se presenta con mayor incidencia en mujeres
jóvenes, de edad media entre 35 a 40 años, sin factores de
riesgo, generalmente relacionada con el embarazo y el puerperio
inmediato.
Se intentó en el
presente trabajo, determinar presencia de eosinófilos en aorta,
a fin de detectar lesiones tempranas que pudiesen contribuir al
desarrollo posterior de disección aórtica.
Esto
permitiría inferir que un aumento en el espesor de la íntima, el
hallazgo de eosinófilos y macrófagos en las túnicas evaluadas,
podrían deberse a la acción de la testosterona, ya que se trata
de ratas jóvenes, de peso normal, no diabéticas, alimentadas
con dieta eumetabólica, que no recibieron ninguna otra
manipulación.
MATERIAL Y MÉTODOS
Se emplearon 30 ratas de la línea “e” eumetabólicas
a partir de los 9 días de edad, acompañadas por 2 madres hasta
el destete.
Las ratas pertenecían al Bioterio Central de de
Facultad de Ciencias Medicas de la Universidad Nacional de
Rosario, criadas en jaulas sin lecho en condiciones de
alternancia luz/oscuridad, alimentadas con Cargill® para
roedores. La colonia tenía status microbiológico no
especificado.
Se las dividió en 2 grupos:
·
Un grupo testigo o control: 10 ratas.
·
Un grupo experimental: 20 ratas.
Al grupo experimental se le inyectó por vía
subcutánea al 9º día de vida, enantato de testosterona 110mg y
propionato de testosterona 25 mg, cuyo solvente es el aceite de
ricino (0.1mg/g de peso).
El grupo control recibió una inyección de aceite de
ricino por vía subcutánea (0.004ml/g de peso).
Las ratas permanecieron en el bioterio hasta ser
trasladadas al laboratorio. Los animales fueron pesados y luego
eutanasiados a los 4 meses de edad bajo campana de éter
ocasionándoles el menor dolor y disconfort respetando las normas
bioéticas.
Se practicó la autopsia a cada animal, se pesó la
grasa retroperitoneal, y los ovarios.
Los ovarios y la aorta fueron fijados en formol
neutro al 10% y se incluyeron en parafina para obtener cortes
histológicos de 5 micrones de espesor. Los cortes se colorearon
con Hematoxilina-Eosina y Giemsa. Se los estudió
microscópicamente y se evaluó:
·
Presencia o ausencia de quistes foliculares
con ausencia de cuerpo lúteo en ovarios.
·
Presencia o ausencia de macrófagos en la
túnica íntima.
·
Presencia o ausencia de eosinófilos y
mastocitos en la túnica media.
·
Presencia o ausencia de eosinófilos y
mastocitos en la túnica adventicia
RESULTADOS
Los ovarios de ratas no tratadas,
presentaron folículos primordiales y folículos en crecimiento,
que se intercalan con cuerpos amarillos voluminosos (Fig. 1).

Fig.1: Rata 400-3,
focalizada de folículos y cuerpo amarillo. 100x
En los animales tratados, con testosterona
se advirtió la presencia de múltiples quistes foliculares,
algunos llamativamente voluminosos y otros con manifiesto
engrosamiento de la capa de las células de la granulosa (Fig.
2).

Fig. 2:
Rata 801-2, poliquistosis ovárica en 40x.
Los animales no tratados, presentaron la
estructura histológica de aorta sin alteraciones (Fig.3).
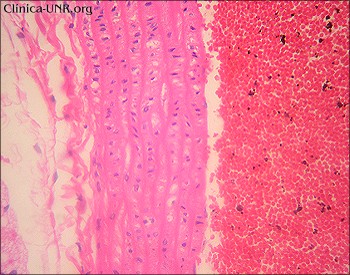
Fig. 3:
Rata 400-1, aorta sin lesiones. 400x.
En la aorta de las ratas tratadas, se
constató la presencia de pequeños cúmulos histiocitarios en la
íntima. En 3 de estas ratas el fenómeno era de grado leve; en
las restantes era más prominente, llegando a producir pequeñas
gibas o mesetas que sobreelevaban el endotelio vascular (Fig.
4).

Fig. 4: Rata 810-1, meseta en íntima aórtica en 400x.
En los animales
tratados no fueron detectados eosinófilos ni mastocitos.
|
Rata |
Aorta |
|
801-1 |
x |
|
801-2 |
x |
|
801-3 |
xx |
|
801-4 |
xxx |
|
810-1 |
xxx |
|
810-2 |
x |
Tabla Nº 1: Cúmulos
histiocitarios en la íntima vascular de arteria aorta.
Referencias: Sin
lesiones: (-)
Pequeños cúmulos histiocitarios: (x)
Pequeños cúmulos histiocitarios con gibas: (xx)
Grandes cúmulos histiocitarios con gibas más grandes: (xxx)
DISCUSIÓN
Es
importante mencionar que si bien se planteó en el proyecto
comenzar con 20 animales, dada una considerable mortandad
sufrida por el grupo experimental, se disidió iniciar otro
plantel más de 10 ratas para dicho grupo. Al finalizar el
trabajo la muestra quedó reducida a: 6 ratas del grupo
experimental y 5 del grupo control.
Los
trabajos que se tomaron como referencia emplearon ratas de la
línea Wistar, y la testosterona fue administrada bajo la forma
de propionato de testosterona y el vehículo utilizado había sido
el aceite de oliva. En este trabajo debimos utilizar un
preparado farmacéutico conformado por enantato de testosterona y
propionato de testosterona cuyo vehículo es el aceite de ricino,
lográndose obtener el desarrollo de poliquistosis ovárica.
Resulta
interesante destacar la diferencia de peso corporal entre los
controles y los experimentales, obteniéndose una media de 257.4g
para los primeros y para los experimentales una media de
227.98g. Al considerar los pesos relativos por 100g de peso
corporal, no hubo diferencias significativas entre la media de
los ovarios del grupo experimental (0.051g) y del grupo control
(0.055g). En cambio, hubo una sensible diferencia en la media de
los pesos relativos de la grasa retroperitoneal: 3.404g para el
grupo experimental versus 3.984g para control. Este último dato
merecería ser estudiado a posteriori, porque contradice algunos
trabajos mencionados en la bibliografía.
Las
lesiones aórticas más marcadas fueron halladas en los animales
que conservaron más alto peso relativo de grasa retroperitoneal.
Este hecho debe ser tomado con prudencia debido al reducido
número de animales empleados, a causa de una importante
mortandad ocurrida durante el transcurso del presente trabajo.
Si bien se
graduó la intensidad de las lesiones histológicas, cabe señalar
que la extensión de las mismas no es grande, por ende, ninguna
de las alteraciones pudo tener repercusiones hemodinámicas de
importancia en los correspondientes territorios. Sin embargo, se
debe considerar la posibilidad de que las lesiones encontradas
puedan magnificarse si se tomaran períodos de estudio más
prolongados.
CONCLUSIÓN
En el
presente proyecto se obtuvo desarrollo de poliquistosis ovárica
tras la inyección de enantato y propionato de testosterona en
ratas de la línea “e”. También se pudo determinar una
interesante diferencia entre los pesos relativos de la grasa
retroperitoneal a favor del grupo control, lo cual contrasta con
algunos trabajos consultados.
En base a
los resultados obtenidos podríamos inferir que las lesiones
encontradas se debieron a la aplicación de testosterona y el
consecuente desarrollo de poliquistosis ovárica, ya que los
animales no recibieron ninguna otra clase de manipulación.
Cabe
mencionar que la muestra final fue muy reducida debido a una
importante mortandad ocurrida durante el transcurso de la
investigación.
BIBLIOGRAFÍA
1)
Jakubowich et al.
Genetic aspects of polycystic ovary syndrome.
Endokrinol Pol. 2005; 56 (3): 285-93.
2)
Luque-Ramirez M. Et al.Genomic
variants in policystyc ovary syndrome. Clin. Chim. Acta. 2006;
366(1-2): 14-26.
3)
Sir-Peterman Teresa et al. Síndrome
Ovario Poliquístico: la importancia de establecer su
diagnóstico. Rev. Med. Chile 2001; 129:
805-812.
4)
Meyer C et al.
Overweight women with polycystic ovary syndrome have evidence of
subclinical cardiovscular disease. J Clin Endocrinol Metab.
2005; 90(10): 5711-6.
5)
Sharma ST et al. Prevention of diabetes and
cardiovascular disease in women with PCOS: treatment with
insulin sensitizers. Best Practice and Research Clinical
Endocrinology and Metabolism. 2006
jun (2): 245-60.
6)
Meyer C et al.
Overweight women with polycystic ovary syndrome have evidence of
subclinical cardiovscular disease. J Clin Endocrinol Metab.
2005; 90(10): 5711-6.
7)
Cussons AJ et al. Cardiovascular disease in
the polycystic ovary syndrome: New insights and perspectivas.
Atherosclerosis 2005; 25: 227-239.
8)
Boulman N. et al.
Increased C-reactive protein levels in the polycystic ovary
syndrome: a marker of cardiovascular disease.
J. Endocrinol. Metab.
2004; 889(5): 2160-5.
9)
Orio F. Jr. et al.
Improvement in endotelial structure and function alter metformin
treatment in young normal-weight women with polycystic ovary
syndrome: results of a 6-month study.
J. Clin Endocrinol. Metab. 2005; 90 (11): 6072-6.
10)
Kravatiri M. J Endocrinol.
Metab. 2005 Sep; 90(9): 5088-95. Predictors
of endotelial disfuction in young women with polycystic ovary
syndrome.
11)
Yilmaz M. et al.
Glucose intolerante, insulin resistance and cardiovascular risk
factors en first degree relatives of women with polycystic ovary
syndrome. Hum. Reprod. 2005; 20 (9): 2414-20.
12)
Kilicdag EB et al. Homocysteine levels in
women with polycystic ovary syndrome treated with metformin
versus rosiglitazone: a randomized study. Hum. Reprod. 2005;
20(4): 894-9.
13)
Haap M. et al. Genetic determinants of
insulin action in polycystic ovary syndrome.
Exp Clin Endocrinol Diabetes 2005; 113 (5):
275-81.
14)
Djuro Macut et al.
Oxidesed low-density lipoprotein concentration-early marker o
fan altered lipid metabolism in young women with PCOS. European
Journal of Endocrinology 2006; 155: 131-136.
15)
Dagre et al.
Association of dehydroepiandrosterone-sulfato with endotelial
function in youngh women with polycystic ovary syndrome.
European J. of Endocrinololgy 2006; 154: 883-890.
16)
Comitee on Care and
Use of laboratory Animal Resources Guide for the Care of
laboratory Animals NIH Publication N° 86-23 Bethesda,
Maryland 985.
|