Discusión del caso clínico. | Presentación |
Inicialmente nuestro paciente se presentó con bicitopenia. El estudio de la bicitopenia está menos explorado que el de la pancitopenia, se define como la reducción de sólo dos linajes celulares: eritrocitos y/o leucocitos y/o plaquetas. En la revista Pathology en el año 2018 fue publicado un estudio realizado con 400 pacientes (pediátricos y adultos) en el mismo: la asociación de anemia con trombocitopenia fue la más frecuente (244 – 61%) y en segundo lugar la asociación de anemia con leucopenia (104 – 26%) como en el caso en discusión y en concordancia con la incidencia evaluada por otros trabajos. (1) Para el grupo etario de nuestro paciente (19-59 años) la etiología más común (58.6%) fue no maligna, 30.6% fue de etiología infecciosa, 4.5% de causa farmacológica y 14% maligna. Se obtuvo una relación estadísticamente significativa entre cada grupo etario y las etiologías mencionadas (p<0,001). En cuanto a las causas infecciosas el dengue fue la principal en este trabajo. (1)
Para el desarrollo de las hipótesis diagnósticas de este caso clínico vamos a utilizar los algoritmos de estudio para pancitopenia. Las pancitopenias se clasifican en forma arbitraria en: CENTRALES y PERIFÉRICAS, según exista o no disminución de las células hematopoyéticas en la médula ósea o un descenso periférico con médula ósea normal. También pueden clasificarse en hereditarias o adquiridas, en el caso en discusión nos referiremos a las causas adquiridas por darse la presentación en un adulto. La división de las pancitopenias en centrales y periféricas en la práctica nunca es tan lineal; por ejemplo, las patologías que infiltran la médula ósea también pueden hacerlo con el bazo. De todos modos, es útil a los fines de organizar el conocimiento a la hora de pensar un paciente con pancitopenia (2).
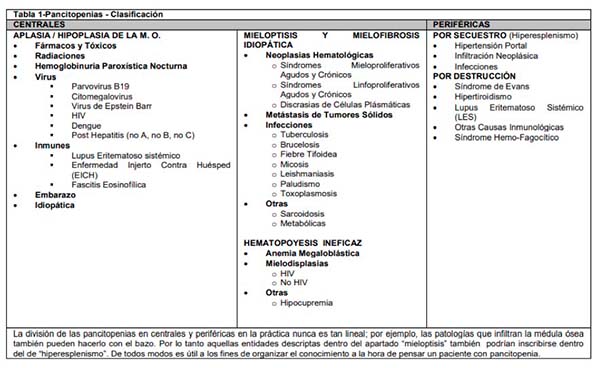
Causas centrales:
- Fármacos y tóxicos: el paciente refiere consumo de drogas por vía inhalatoria como la cocaína. Fue ampliamente reportada la agranulocitosis secundaria a consumo de cocaína adulterada con levamisol(3). Ha sido reportada también en Argentina (4) en asociación a vasculitis cutánea y agranulocitosis (5). La Facultad de Medicina de Illinois publicó un reporte de caso en el año 2016 de lesiones cutáneas secundarias a cocaína (CIMDL -Cocaine Induced Midline Destructive Lesions) en el que se observaron lesiones extranasales, en los que el resultado de la biopsia mostró infiltrado submucoso de neutrófilos y células plasmáticas sin vasculitis ni trombosis. En las lesiones inducidas por cocaína se observa habitualmente ANCA-P positivo, lo que tendría utilidad en el diagnóstico diferencial entre granulomatosis con poliangeítis (ANCA-C) ya que la distinción histológica es más dificultosa (6)
- Síndromes de fallo medular:
o Anemia aplásica adquirida: síndrome caracterizado por pancitopenia periférica y médula ósea hipocelular junto con el compromiso de al menos 2 líneas celulares en sangre periférica. Debe descartarse etiología viral y otros diagnósticos compatibles con fallo medular.
o Hemoglobinuria paroxística nocturna: presenta 4 manifestaciones clásicas: anemia por hemólisis intravascular, los episodios de hemoglobinuria, la leucopenia y/o plaquetopenias acompañantes que son de grado variable y las trombosis, con frecuencia en sitios inusuales. La técnica de elección para el diagnóstico es la citometría de flujo y no estaría indicada en este momento la búsqueda del clon en nuestro paciente ya que no presenta hemólisis ni hemoglobinuria y hay otras causas que pueden explicar la pancitopenia.
- Infecciones virales:
o Parvovirus B19: la enfermedad por parvovirus B19 es infrecuente en el adulto y está poco descripta en la literatura, afecta en mayor medida a mujeres en la cuarta y quinta décadas de la vida, y se manifiesta con: fiebre, poliartralgias periféricas, simétricas, exantema, lesiones cutáneas tipo purpúricas. En pacientes con factores de riesgo puede desencadenar eventos graves tales como crisis aplásicas y anemia severa entre otras (9). El Hospital General Universitario de La Paz Madrid realizó un estudio retrospectivo en el año 2014 donde incluyeron aquellos adultos que habían padecido infección aguda por parvovirus B19 en el año 2012. El hallazgo clínico más prevalente en el estudio fueron las lesiones cutáneas siendo purpúricas (55%) y un 10% fueron vasculitis. En cuanto a alteraciones hematológicas 12% presentó anemia leve, 30% presento alteraciones de la serie blanca (linfopenia, monocitosis y neutrofilia) y el 6% (sólo 3 pacientes) trombocitosis (11).
o Citomegalovirus (CMV): la enfermedad por CMV puede imitar una gran cantidad de diagnósticos diferenciales y convertirse en un desafío diagnóstico, especialmente en adultos inmunocompetentes, lo que conlleva a retraso en el diagnóstico, aumento de la morbi-mortalidad y del gasto sanitario. En la mayoría de los casos se manifiesta con un cuadro mononucleosis like (fiebre, astenia, faringitis, adenopatía (cervical) y hepatitis). Cabe destacar que como en algunos reportes de caso, si bien se ha obtenido resultado positivo para CMV resulta difícil caracterizar el rol patógeno del mismo en pacientes inmunocompetentes (13). Un artículo publicado en la revista The American Journal of Dermatology titulado “Infección cutánea por citomegalovirus en un paciente inmunocompetente: ¿espectador inocente o culpable?” reportan el caso de una paciente con lesión ulcerada la región pretibial sin respuesta a antibióticos, con biopsia e inmunohistoquímica compatibles con CMV, en la que no se obtuvo respuesta frente al tratamiento de elección por lo que no se logró identificar el rol patógeno del CMV. Hasta en un 3% de los casos la PCR puede ser negativa por lo que no lo descarta.
o Virus Epstein Barr (VEB): en adultos frecuentemente produce un síndrome mononucleosis like: el 50% de los pacientes se presentan con la tríada: fiebre, linfadenopatía y faringitis, además esplenomegalia, petequias en el paladar y hepatomegalia en el 10% de los pacientes al menos. Otras complicaciones menos frecuentes son: anemia hemolítica, anemia aplásica, trombocitopenia, miocarditis, úlceras genitales y síntomas neurológicos (meningoencefalitis). Fuertemente asociado a la presencia de neoplasias, sólidas como oncohematológicas (14).
o Dengue: es improbable que sea la causa porque no tiene las manifestaciones clínicas típicas (mialgias, artralgias), ni explicaría las lesiones cutáneas y en cuanto a las alteraciones analíticas no se observó hemoconcentración a pesar de contar con leucopenia.
o Post hepatitis: serologías negativas
- Inmunes
o Lupus eritematoso sistémico: Fan negativo.
- Neoplasias hematológicas: si bien presenta bicitopenia, la misma no es de la profundidad observada habitualmente en las neoplasias hematológicas, el paciente no tiene hepatoesplenomegalia y tampoco linfadenopatías sugestivas de las mismas. Se encuentra pendiente la realización de punción aspirativa de médula ósea con objetivo diagnóstico.
En el año 2019 fue publicado otro trabajo que intentó demostrar que la severidad de las citopenias podría ser de utilidad para diferenciar los trastornos primarios de los trastornos secundarios. (15)
Cuando se examinan fisiopatológicamente, las citopenias pueden deberse a hematopoyesis ineficaz, infiltración de médula ósea, secuestro periférico y mediada por destrucción. Como resultado del estudio se obtuvo una relación estadísticamente significativa (2) entre la severidad de las citopenias y la etiología primaria como podemos ver en la siguiente tabla:
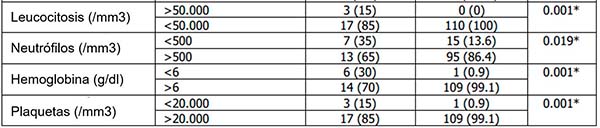
En los pacientes con causa primaria: el recuento de neutrófilos fue menor a 500 en el 35% de los casos, un 65% presentó neutrófilos mayores a 500; mientras que en los pacientes con causa secundaria el 86% tenía valores por encima de 500. En cuanto a la anemia, en los pacientes con etiología primaria el 70% tenía hemoglobina mayor a 6 g/dl mientras que en etiología secundaria el 99.1% de los pacientes tenían hemoglobina mayor a 6 g/dl. (2)
Causas periféricas
- Por destrucción
o Hipertiroidismo: (Perfil tiroideo normal)
o Síndrome hemofagocítico (SHF): su mecanismo de destrucción celular está caracterizado por una proliferación incontrolada de histiocitos en médula ósea, ganglios e hígado y bazo, con una intensa actividad fagocítica de células hematopoyéticas. El SHF puede ser primario o secundario (reactivo) y aparecer durante el curso de numerosas enfermedades (ver tabla).

Clínicamente se caracteriza por la presencia de fiebre, bicitopenia o pancitopenia, hepatoesplenomegalia, adenopatías, trastornos funcionales hepáticos, mialgias y alteraciones de la coagulación. En el laboratorio se puede observar pancitopenia con parámetros de hemólisis. La médula ósea es el principal lugar de afección, pudiendo ser hipocelular, normocelular o hipercelular. En la siguiente tabla se enumeran los criterios diagnósticos para el SHF.

El paciente en discusión se presentó con fiebre, citopenias, tiene hipertrigliceridemia pero menor a 265 y ferritina mayor a 500, y debiera reunir al menos 5 de estos criterios para establecer el diagnóstico de acuerdo a la tabla.
�Las lesiones cutáneas encontradas en el paciente en discusión son lesiones secundarias, concretamente úlceras, por lo que describiré posibles causas de las mismas a continuación.
INFLAMATORIAS:
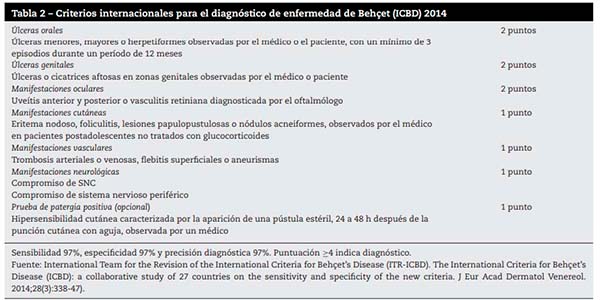
- Behçet: en la enfermedad de Behçet las lesiones cutáneas son el sello distintivo de la patología y, además, sus manifestaciones iniciales más frecuentes. El paciente en discusión si bien presenta lesiones orales y genitales, no cuenta con compromiso ocular, ni vascular, ni neurológico con lo que no contaría con los criterios diagnósticos (ver tabla). ¿Y la bicitopenia? (16,17) Desde el punto de vista hematológico la enfermedad de Behcet a menudo se acompaña de leucocitosis, rara vez de citopenias, pero puede evolucionar o presentar como complicación la aparición de un síndrome mielodisplásico (17). En este reporte de caso de una paciente coreana, destacan la dificultad para acceder al diagnóstico y la demora en realizar la punción aspirativa de médula ósea (1 año después) por haberse presentado en forma inicial como bicitopenia que fue atribuida solo a la enfermedad de Behcet(18).
- Vasculitis ANCA positivas: ¿Qué valor tiene el ANCA positivo? Las vasculitis primarias son patologías complejas, con manifestaciones clínicas variadas, las que pueden ser comunes a las que se presentan en múltiples enfermedades. Los anticuerpos anticitoplasma de neutrófilo (ANCA) constituyeron una revolución en el diagnóstico y la investigación de estas enfermedades, al ser el primer, y hasta ahora único, biomarcador para tres de estas patologías que afectan vasos de calibre pequeño. Desde su descripción, mucho se ha avanzado, pero aún hay aspectos poco claros o mal entendidos en cuanto a su mejor uso en la clínica. Ello puede llevar a errores como hacer de esta prueba un sinónimo de la existencia de vasculitis, o a sobreestimar su relevancia. En la siguiente tabla podemos observar otras patologías con resultados positivos para ANCA (19).

o PAM Poliangitis microscópica: vasculitis de pequeño y mediano calibre. El curso de la enfermedad puede ser lento con síntomas sistémicos recurrentes (fiebre, pérdida de peso, dolor articular, muscular), púrpura palpable en el 50% de los pacientes y alteración de la función renal o glomerulonefritis con o sin compromiso pulmonar.
o Granulomatosis con poliangitis: inflamación granulomatosa necrotizante localizada por lo general en vías aéreas superiores e inferiores, y vasculitis de pequeños y medianos vasos. Como manifestaciones en común con el caso presentado: reducción de los conductos nasales, ulceraciones, secreción purulenta, perforación del tabique nasal (cabe destacar que el paciente es consumidor de cocaína). En cuanto a la analítica habitualmente cursa con anemia, pero con leucocitosis.
- Sarcoidosis: enfermedad sistémica granulomatosa de etiología desconocida que se presenta más frecuentemente con adenopatías hiliares y alteración del parénquima pulmonar, en los focos de actividad de la enfermedad se acumulan linfocitos T helper 1 y macrófagos formando granulomas no caseificantes. El espectro de lesiones cutáneas secundarias a sarcoidosis es francamente amplio: eritema nodoso, lesiones papulares, maculopapulares, nódulos subcutáneos, despigmentación, eritema y úlceras. La bicitopenia con anemia y leucopenia es un hallazgo analítico frecuente en esta entidad.
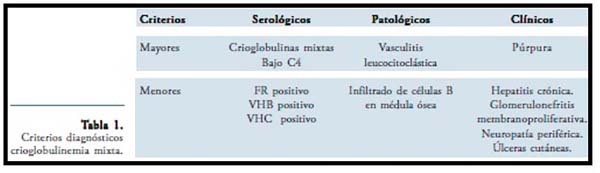
- Crioglobulinemia: está definida por la persistencia en suero de inmunoglobulinas anormales. Sus manifestaciones clínicas pueden ser: osteoarticulares, neurológicas, renales y cutáneas con lesiones tipo úlceras necróticas. Los criterios clínicos expuestos en la siguiente tabla incluyen: criterios serológicos, el paciente en discusión cuenta sólo con consumo de complemento C4, no se han solicitado a la fecha crioglobulinas en sangre, no contamos con resultado de biopsia cutánea por el momento y en cuanto a las manifestaciones clínicas, por presentar úlceras cumpliría con uno de los criterios menores.
NEOPLASIA
- Las úlceras tumorales son infiltraciones cutáneas de células cancerígenas. Generalmente se producen por el crecimiento de un tumor primario de la piel (carcinoma basocelular, carcinoma de células escamosas, melanoma, sarcoma de Kaposi, linfomas cutáneos) o por metástasis (invasión de la piel por otros tumores, los más comunes de mama, cabeza y cuello, pulmón, abdomen y genitales). Suelen aparecer en pacientes durante la fase terminal del cáncer y/o en el desarrollo de tumores de alto grado de malignidad.
- Pareneoplásico: como el pioderma gangrenoso y el síndrome de Sweet, que son asimismo entidades inflamatorias, pero que presentan lesiones cutáneas diferentes a las de nuestro paciente.
INFECCIOSAS
- Bacterianas (20): estas lesiones no pueden explicar en forma completa el cuadro clínico teniendo en consideración la bicitopenia. Además, el paciente se encuentra con un esquema terapéutico de amplio espectro, habiendo realizado ya previamente otros tratamientos antibióticos ambulatorios sin respuesta.
- Micosis profundas:
o Histoplasmosis (Histoplasma capsulatum): la población de riesgo para desarrollar histoplasmosis diseminada son pacientes inmunocomprometidos, y dentro de ellos el principal grupo es el de infectados por VIH con recuentos de linfocitos CD4 por debajo de 150 a 200 células por mm3 (21), además de pacientes con neoplasias linfoproliferativas y aquellos que reciben terapia con corticoides citotóxicos e inmunosupresores aunque existen varios reportes de casos publicados en la literatura de pacientes inmunocompetentes que desarrollan cuadros de histoplasmosis diseminada. Este cuadro podría explicar además la bicitopenia por compromiso de medula ósea. Fue reportado en el año 2012 (21) el diagnóstico de histoplasmosis diseminada en paciente inmunocompetente con lesiones orales y
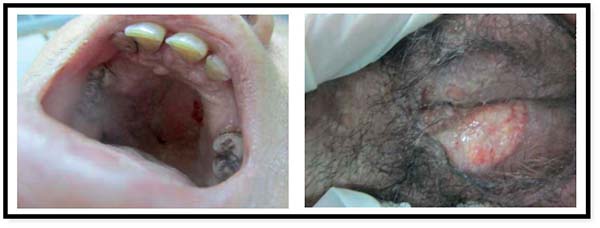
o Tuberculosis (22): considerando que el paciente en discusión no presenta alteraciones en el parénquima pulmonar estaríamos frente a tuberculosis cutánea, que constituyen entre el 1-2% de los casos de tuberculosis. Tiene noción de foco positiva ya que estuvo privado de su libertad durante 12 años. También explicaría las citopenias.
o Lepra: es de evolución subaguda, crónica y las lesiones habituales no son compatibles con las de nuestro paciente en ninguno de los estadios evolutivos de la enfermedad (22).
Consideraciones finales
Como consideraciones finales me planteo los siguientes interrogantes:
- ¿Qué fue primero, la neutropenia o las lesiones cutáneas? ¿Se trata de agranulocitosis secundaria a fármacos (como el levamisol) que condujo a inmunosupresión y posterior aparición de infección oportunista? ¿Había compromiso de M.O. de origen primario previo a la aparición de las lesiones? O ¿estamos frente a una infección que produjo infiltración de médula ósea y en la que la bicitopenia es una mera consecuencia?
- ¿Podemos establecer una hipótesis propia del modelo unicausal, que logre explicar todas las manifestaciones: la bicitopenia y las lesiones cutáneas? Considero que sólo 2 de las mencionadas hasta ahora tienen ese poder explicativo:
o Vasculitis inducida por cocaína, coincidente también con la remisión de la neutropenia en contexto del abandono del tóxico y la mejoría parcial de las lesiones.
o Micosis profunda diseminada: fundamentalmente histoplasmosis, aunque difícilmente podría explicar la remisión de la citopenia y la mejoría parcial de las lesiones cutáneas sin tratamiento dirigido para las mismas.
- El paciente recibió tratamiento con piperacilina tazobactam, vancomicina y Aciclovir, ¿qué rol jugaron los antibióticos en la evolución clínica? ¿Las heridas mejoraron en conjunto con el control del dolor por tratamiento de sobreinfección bacteriana? ¿Debería continuarlos o suspenderlos?
Considero que el resultado de la biopsia cutánea puede ser de gran valor, fundamentalmente para la definición del curso terapéutico a seguir.
En caso de confirmar lesiones de tipo vasculitis, o que no pudiera descartarse que las lesiones sean inducidas por cocaína podría realizarse una prueba terapéutica con corticoesteroides.
La punción aspirativa de médula ósea tendría utilidad para confirmar o desestimar los diagnósticos mencionados por lo que considero que debe realizarse a la brevedad.
Por último, independientemente de si se trate o no de la causa del cuadro actual, considero pertinente establecer una estrategia multidisciplinaria para deshabituación de cocaína
�Bibliografía:
1. Singh, A., Hungund, B., Kumar, L., & Pattanshetti, M. (2018). Clinico-haematological profile of patients with bicytopenia. Pathology, 50(5), 540–548. https://doi.org/10.1016/j.pathol.2018.03.008
2. Severini, J, Tardío, C., Tardío, M., Cusumano, M., Dolce, V., Perotti, D., Grossi, G., Trivisonno, F., Miljevic, J. (2010). Abordaje del paciente con pancitopenia. Publicación digital de la 1ra Cátedra de Clínica Médica y Terapéutica y la Carrera de Posgrado de especialización en Clínica Médica
3. Buchanan, J. A., & Lavonas, E. J. (2012). Agranulocytosis and other consequences due to use of illicit cocaine contaminated with levamisole. Current opinion in hematology, 19(1), 27–31. https://doi.org/10.1097/MOH.0b013e32834da9ef
4. Calligaris M., Nipoti J., Gorosito M., Garrido M.G., Fernandez Bussy R.A. (2017). Casos clínicos: vasculitis inducida por cocaína. Dermatología Argentina Vol. 23 nª 4: 196-198 ISSN 1515-8411.
5. Pellegrini D., Young P., Grosso V., Massa M., Bruetman J. E. (2013) Agranulocitosis por levamisole asociado a cocaína. Servicio de Clínica Médica, Hospital Británico de Buenos Aires Revista Medicina Nª5 – Buenos Aires. 73: 464-466
6. Blaise, B., Buescher, L., & Wilson, M. L. (2016). Multiple mucocutaneous ulcers associated with cocaine-induced midline destructive lesions. Dermatology online journal, 22(9), 13030/qt9zw361qb.
7. Schieppati, Francesca; Gregorini, Gina; Hummel, Amber M.; D'Adda, Mariella; Borlenghi, Erika; Lamorgese, Cinzia; Specks, Ulrich; Rossi, Giuseppe (2018). Acquired cyclic neutropenia associated with cocaine-induced anti-neutrophil cytoplasmic antibodies binding to human neutrophil elastase (HNE-ANCA). American Journal of Hematology, (), –. doi:10.1002/ajh.25197
8. Liaqat, Hassan; Shirvanian, Narine; Ammad Ud Din, Mohammad; Amin, Ali (2020). Cocaineâ?�related vasculitis. Clinical Case Reports, 8(12), 3640–3641. doi:10.1002/ccr3.3450
9. Rodriguez Bandera A. I., Arenal M., Vorlicka K., Ruiz Bravo-Burguillos E., Montero Vega D., Vidaurrázaga Diaz-Arcava C. (2014) Estudio retrospectivo de 49 casos de infección aguda por parvovirus b19 en adultos. Hospital Universitario La Paz, Madrid, España.
10. Lancini, D., Faddy, H. M., Flower, R., & Hogan, C. (2014). Cytomegalovirus disease in immunocompetent adults. The Medical journal of Australia, 201(10), 578–580. https://doi.org/10.5694/mja14.00183
11. Grushchak, S., Hutchens, K. A., Joy, C., Peterson, A., Speiser, J., & Mudaliar, K. (2018). Cutaneous Cytomegalovirus Infection in an Immunocompetent Patient: Innocent Bystander or Culprit?. The American Journal of dermatopathology, 40(4), 295–298. https://doi.org/10.1097/DAD.0000000000001009
12. Cohen, Jeffrey I. (2000). Epstein–Barr Virus Infection. New England Journal of Medicine, 343(7), 481–492. doi:10.1056/NEJM200008173430707
13. Hatemi, G., Seyahi, E., Fresko, I., Talarico, R., & Hamuryudan, V. (2020). One year in review 2020: Behçet's syndrome. Clinical and experimental rheumatology, 38 Suppl 127(5), 3–10.
14. Bettiol, A., Prisco, D., & Emmi, G. (2020). Behçet: the syndrome. Rheumatology (Oxford, England), 59(Suppl 3), iii101–iii107. https://doi.org/10.1093/rheumatology/kez626
15. Sarbay H. (2019). Comparison of the severity of cytopenias with etiologic factors in patients with pancytopenia and bicytopenia. The Pan African medical journal, 34, 149. https://doi.org/10.11604/pamj.2019.34.149.18749
16. Arimura, K., Arima, N., Matsushita, K., Akimoto, M., Park, C. Y., Uozumi, K., & Tei, C. (2007). High incidence of morphological myelodysplasia and apoptotic bone marrow cells in Behçet's disease. Journal of clinical immunology, 27(2), 145–151. https://doi.org/10.1007/s10875-006-9064-9
17. Ohno E, Ohtsuka E, Watanabe K, Kohno T, Takaoka K, Saburi Y, Kikuchi H, Nasu M. Behcet’s disease associated with myelodysplastic syndromes. Cancer 79:262–268, 1997
18. Karuvannur S, Lipstein E, Brennessel D, Rosner F. Atypical Behc¸et’s syndrome in a patient with myelodysplastic syndrome. Mount Sinai J Med 68:403–405, 2001
19. Luis Felipe Flores-Suárez (2012). Utilidad de los anticuerpos anticitoplasma de neutrófilo en reumatología Reumatología Clínica Volume 8, Issue 6, Pages 351-357, ISSN 1699-258X, https://doi.org/10.1016/j.reuma.2012.03.002.
20. Zaballos P.D., Ara Martín M., Sanz Colomo B. El chancroide (2002). Centro de Prevención y Control de las ETS. CAP Les Drassanes. Barcelona. Piel 17(6):242-53
21. Martinez Braga G., Agûero Zaputovich F., Di Martino Ortiz B., Bolla de Lezcano L. Úlceras orales y genitales como presentación de histoplasmosis diseminada en paciente inmunocompetente. Reporte de un caso. 2012. Dermatol Venez. Vol.50. Nº1
22. Franco-Paredes, C., Marcos, L. A., Henao-Martínez, A. F., Rodríguez-Morales, A. J., Villamil-Gómez, W. E., Gotuzzo, E., & Bonifaz, A. (2018). Cutaneous Mycobacterial Infections. Clinical microbiology reviews, 32(1), e00069-18. https://doi.org/10.1128/CMR.00069-18
23. Ramos C. et al. Paracoccidiodiomicosis diseminada juvenil. 2007. Folia dermatol. Peru; 18 (3): 140-146.
|
Imágenes del caso
|